近日,浙江大学基础交叉研究院交叉原创板块成员、化学系唐睿康教授联合基础医学院陈晓教授、茵梓教授及浙大二院沈炜亮主任医师团队,在Science Translational Medicine发表题为“A bioinspired mineralized collagen scaffold promotes enthesis healing and activates Gli1 expression in preclinical models”的研究成果。
全球每年有超过150万例的肩袖、交叉韧带等腱骨损伤修复手术,面临着一个根本性临床难题:外科缝合虽能实现力学固定,却无法在肌腱(软)与骨骼(硬)之间重建具有生物活性的纤维软骨过渡层。由于缺失这一关键的“生物接口”,修复组织常由瘢痕纤维化胶原替代,导致术后再撕裂率高、功能恢复不理想。其根源在于长期以来对腱骨连接处的纤维软骨胶原在纳米尺度的精确构成及其再生所需的定量化生物材料参数缺乏深入认知。
针对这一难题,研究团队首次在2-3纳米分辨率下解码了纤维软骨的正常胶原内矿化三维结构,发现了驱动纤维软骨再生的精确无机物含量阈值(33%)。为攻克如何精准复刻该仿生结构的瓶颈问题,研究团队充分发挥唐睿康、潘海华团队在胶原矿化科技领域的技术优势,基于磷酸钙团簇仿生矿化技术,历经4年开发,成功创制出符合该“黄金比例”的仿生矿化胶原支架。在小鼠、大鼠、兔及山羊等多物种模型中,该支架有效逆转了瘢痕纤维化胶原沉积,实现了优越的纤维软骨再生与功能恢复,标志着腱骨修复从“机械固定”向“生物融合”迈出了关键一步。
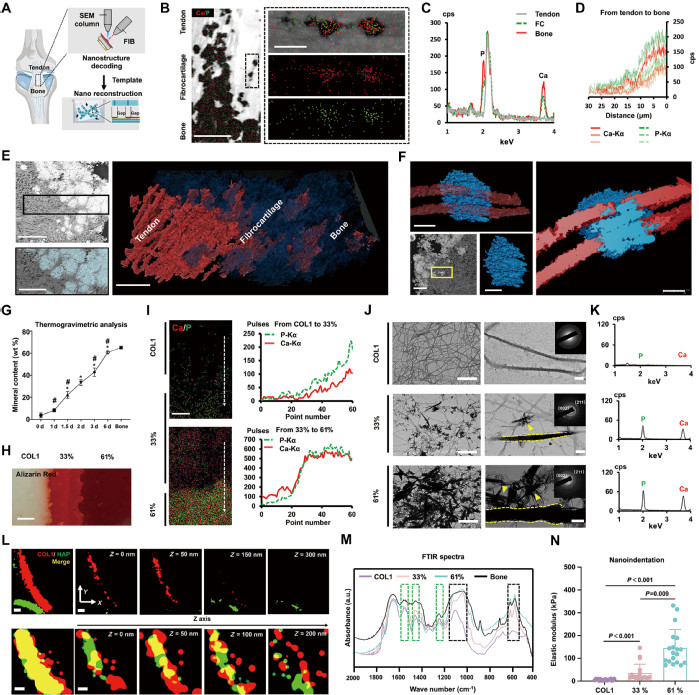
在1-3纳米尺度上对纤维软骨进行解码和仿生重建
原文链接:https://doi.org/10.1126/scitranslmed.ado6948

 Search
Search

